香港大学团队提出一种全新低侵袭脑电极“覆盖脑表面电极薄膜”,只需在头骨开出数毫米小孔,把折叠电极送入颅内再以导丝展开,成功覆盖较大脑表面区域并稳定量度脑电信号。研究以比格犬作测试,示范设备可在约2小时内以标准脑外科工具完成植入,犬只翌日已可正常活动,显示安全性具潜力。
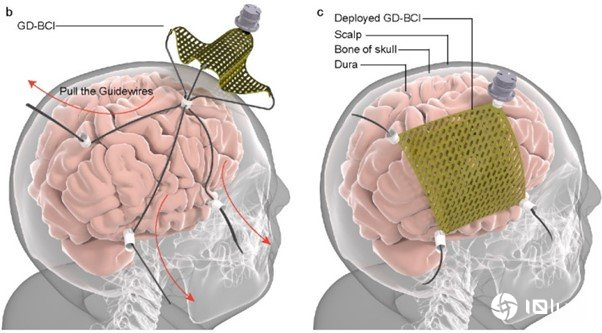
论文由香港大学机械工程系及医学界多名研究人员合作,在arXiv公开。团队提出“guidewire-driven deployable ECoG array”概念,把高密度ECoG电极制成超薄柔性薄膜,折叠后经直径约4至8mm头骨孔送入颅内,再以多样导丝从其余小孔拉动,把电极在硬膜表面展开。电极数组采用约21μm厚薄膜基材,在约2 x 2cm面积内集成256个电极,兼顾柔韧度与机械强度,在展开过程保持贴附脑表面并维持良好接触阻抗。
研究团队先在人工脑模型上测试展开机构与机械可靠性,模拟显示即使出现拉扯失误,破损多发生在导丝与数组边缘连接位置,实际电极接触点一般可维持完整,降低功能损失风险。相关设计也参考以往以软性机械设备或柔性电极经小开孔展开ECoG数组的研究,但这次方案采用更薄薄膜与简化导丝机构,目标是方便在常规脑外科环境中应用。
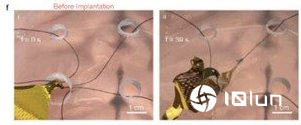
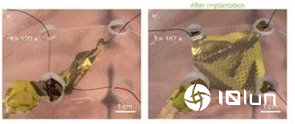
在示范手术中,医生先在头盖骨钻出一个约8mm孔作主入路,再在邻近位置开3个约4mm小孔,作为导丝出口与固定点。医生把折叠电极从8mm孔推入硬膜外空间,再逐一把电极四角导丝牵引出3个小孔,通过拉动导丝令薄膜在硬膜表面摊开成预定形状并定位,过程使用标准脑外科器械约2小时可完成。
这种入路与传统需大范围开颅放置硬膜下或皮层表面电极方式相比,大幅缩小开骨范围,理论上可减少脑肿胀、炎症及感染等并发症机会,与近年通过小钻孔植入ECoG或立体脑电图电极趋势一致。研究也指出电极经硬膜外(epidural)放置配合高密度设计,尝试在信号品质与侵袭程度之间取得较佳平衡。
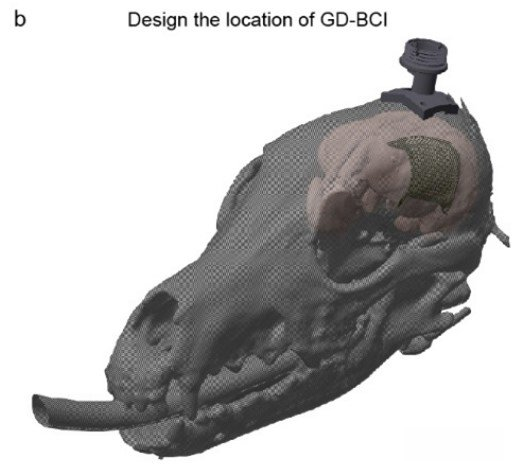
团队选用比格犬作动物实验,把电极数组放在犬只听觉皮层区域硬膜上,并播放100Hz、1,000Hz及10,000Hz三种不同频率声音,记录对应脑电活动。分析结果显示,不同频率声音会在电极数组上产生截然不同空间与时间图样,显示设备可捕捉到与听觉加工有关的高品质ECoG信号。
研究团队进一步把量度到的神经信号输入机器学习模型,利用多种常见分类算法,对“听到哪一种频率声音”进行判别,整体分类准确率超过80%,验证数组在实际BCI解码任务中具实用潜力。植入后监察显示,多数电极在1kHz下阻抗低于100kΩ,比例约达97.7%,反映电极在实验期间维持稳定电接触与信号品质。
在安全性方面,团队以MRI关注犬只脑部变化,在手术后即时及2星期时段检查脑结构,未见显著异常变化,也没有明显出血或肿胀迹象。犬只在手术翌日已恢复正常活动,被视为术式侵袭性相对较低的证据之一,与传统需要大面积开颅植入电极手术后需较长住院观察时间形成对比。
相关结果呼应以往针对较少接触点电极或小规模ECoG经钻孔植入研究,有指若能控制开孔大小并保持硬膜完整,患者或动物在恢复期承受风险可明显下降。研究人员也强调,新系统在设计时兼顾生物兼容性,期望在慢性长期监测场景中仍可维持稳定,而不单只作短期实验用途。
论文指出,这种可经小孔展开的高密度ECoG数组技术,将来有望用于多类脑相关医疗与BCI应用,例如对现有人工耳蜗不适用患者提供新型听觉辅助方案,直接在脑听觉皮层植入电极接收声音编码信号。同时高密度、广覆盖ECoG对以“意念控制”外骨骼或机械手臂等运动BCI系统来说也甚关键,可提升指令解析精确度,减少对深部电极或大范围开颅需求。
在癫痫等脑部疾病诊断与治疗方面,若能以较低风险方式长时间监测大面积皮层活动,有助更精细地定位癫痫放电起始区域,为之后手术切除或精准刺激治疗提供更准确图谱。外国已有多篇文献讨论经血管或小开孔方式实现低侵袭BCI,香港团队这次研究为“导丝驱动电极展开”路线提供实证,未来若在人体临床试验上证明安全有效,或可成为新一代BCI植入方案重要选项之一。
数据源:Arxiv
本网通过AI自动登载内容,本文转载自MSN,【提供者:十轮网科技资讯 | 作者:佚名】,仅代表原作者个人观点。本站旨在传播优质文章,无商业用途。如不想在本站展示可联系删除。